- Prevádzka: automatická, riadená PLC
- Pomôcky: Na výrobu 1 000 Nm³/h H2zo zemného plynu sú potrebné tieto služby:
- 380-420 Nm³/h zemného plynu
- 900 kg/h napájacej vody kotla
- Elektrický výkon 28 kW
- 38 m³/h chladiacej vody *
- * môže byť nahradené chladením vzduchom
- Vedľajší produkt: export pary, ak je to potrebné
Video
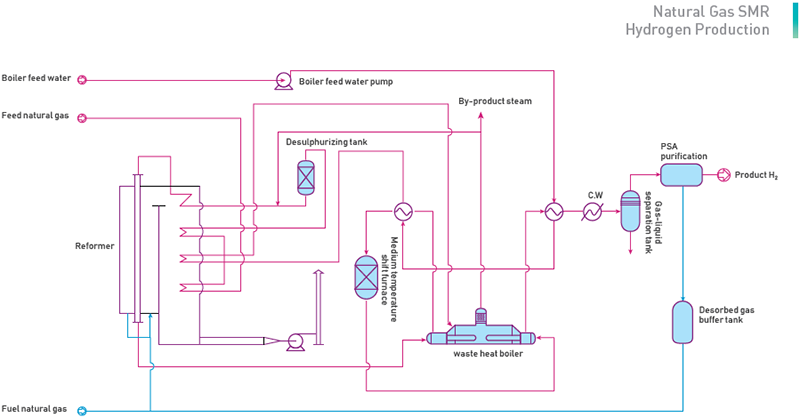
Výroba vodíka zo zemného plynu spočíva v chemickej reakcii stlačeného a odsíreného zemného plynu a pary v špeciálnom reformátore naplnenom katalyzátorom a generovanie reformovacieho plynu s H2, CO2 a CO, premena CO v reformovacích plynoch na CO₂ a následná extrakcia. kvalifikovaný H2 z reformovacích plynov adsorpciou pri kolísaní tlaku (PSA).
Návrh závodu na výrobu vodíka a výber zariadení je výsledkom rozsiahlych inžinierskych štúdií TCWY a hodnotení dodávateľov, pričom sa optimalizovali najmä nasledovné:
1. Bezpečnosť a jednoduchosť obsluhy
2. Spoľahlivosť
3. Krátka dodávka vybavenia
4. Minimálna práca v teréne
5. Konkurenčné kapitálové a prevádzkové náklady
(1) Odsírenie zemného plynu
Pri určitej teplote a tlaku, s privádzaným plynom prostredníctvom oxidácie adsorbentu mangánu a oxidu zinočnatého, bude celková síra v privádzanom plyne nižšia ako 0,2 ppm, aby sa splnili požiadavky katalyzátorov na parný reforming.
Hlavná reakcia je:
| COS + MnO |
| MnS+H2O |
| H2S+ZnO |
(2) Parná reforma NG
Proces parného reformovania využíva vodnú paru ako oxidant a pomocou niklového katalyzátora sa uhľovodíky pretvoria na surový plyn na výrobu plynného vodíka. Tento proces je endotermický proces, ktorý vyžaduje dodávku tepla zo sálavej časti pece.
Hlavná reakcia v prítomnosti niklových katalyzátorov je nasledovná:
| CnHm+nH2O = nCO+(n+m/2)H2 |
| CO+H2O = CO2+H2 △H°298= – 41 KJ/mol |
| CO+3H2 = CH4+H2O△H°298= – 206 KJ/mol |
(3) Purifikácia PSA
Ako proces chemickej jednotky sa technológia separácie plynov PSA rýchlo rozvíja na nezávislú disciplínu a čoraz viac sa používa v oblastiach petrochémie, chémie, hutníctva, elektroniky, národnej obrany, medicíny, ľahkého priemyslu, poľnohospodárstva a ochrany životného prostredia. odvetviach atď. V súčasnosti sa PSA stalo hlavným procesom H2separácia, ktorá sa úspešne používa na čistenie a separáciu oxidu uhličitého, oxidu uhoľnatého, dusíka, kyslíka, metánu a iných priemyselných plynov.
Štúdia zistila, že niektoré pevné materiály s dobrou poréznou štruktúrou môžu absorbovať molekuly tekutiny a takýto absorpčný materiál sa nazýva absorbent. Keď sa molekuly tekutiny dostanú do kontaktu s pevnými adsorbentmi, adsorpcia nastane okamžite. Výsledkom adsorpcie je rozdielna koncentrácia absorbovaných molekúl v tekutine a na absorpčnom povrchu. A adsorbované molekuly absorbentom budú obohatené na jeho povrchu. Ako obvykle, rôzne molekuly budú vykazovať rôzne charakteristiky, keď sú absorbované adsorbentmi. Priamo to ovplyvnia aj vonkajšie podmienky, ako je teplota a koncentrácia tekutiny (tlak). Preto práve vďaka tomuto druhu odlišných charakteristík, zmenou teploty alebo tlaku, môžeme dosiahnuť separáciu a čistenie zmesi.
Pre túto rastlinu sa do adsorpčného lôžka plnia rôzne adsorbenty. Keď reformovací plyn (zmes plynov) prúdi do adsorpčnej kolóny (adsorpčného lôžka) pod určitým tlakom, v dôsledku rôznych adsorpčných charakteristík H2, CO, CH2, CO2atď. CO, CH2a CO2sú adsorbované adsorbentmi, zatiaľ čo H2bude vytekať z hornej časti lôžka, aby sa získal kvalifikovaný produktový vodík.










 MnS+CO2
MnS+CO2









